Vilniaus universiteto (VU) Gyvybės mokslų centro (GMC) Biochemijos instituto Proteomikos centro mokslininkai, vadovaujami dr. Mindaugo Valiaus, kartu su VU ligoninės Santaros klinikų gydytojais siekia įveikti vieną sudėtingiausių šiuolaikinės medicinos iššūkių, susijusių su kasos vėžiu. Tarpdisciplininio bendradarbiavimo tikslas – sujungti pažangius molekulinius tyrimus ir klinikinę praktiką, ieškant efektyvesnių, pacientui pritaikytų gydymo sprendimų.
Kasos vėžys išlieka viena mirtiniausių ligų
Kasos vėžys yra viena iš didžiausiu mirtingumu pasižyminčių onkologinių ligų Europoje ir pasaulyje. Jis vadinamas „tyliuoju“ vėžiu, nes dažnai pacientai į gydytojus kreipiasi tik tada, kai liga jau pažengusi ir jos gydymo galimybės ribotos. Lietuvoje apie 80 proc. kasos vėžio atvejų diagnozuojama vėlyvose stadijose, penkerius metus išgyvena vos keli procentai.
Pasaulyje ši liga pasiglemžė tokių garsenybių kaip „Apple“ įkūrėjas Steve’as Jobsas, aktoriai Alanas Rickmanas ir Patrickas Swayze’as, operos legenda Luciano Pavarotti gyvybes.
Daugeliui kitų vėžio atmainų jau yra sukurti kartais itin brangūs, bet efektyvūs gydymo metodai, o kasos vėžiui gydyti tokių metodų beveik nėra. Nepaisant medicinos pažangos, kasos vėžio gydymo rezultatai per pastaruosius dešimtmečius gerėjo lėčiausiai tarp visų kitų dažniausių onkologinių ligų.
Kaip kasos vėžys gydomas šiandien?
Santaros klinikose kasos vėžio gydymas grindžiamas tarptautinėmis gairėmis ir individualiu paciento būklės vertinimu.
„Nors pagrindinis gydymo būdas yra chirurgija, vien operacijos dažniausiai nepakanka – gydymas papildomas chemoterapija prieš operaciją arba po jos, o kai kuriais atvejais ir spinduline terapija“, – sako vienas projekto dalyvių, abdominalinės chirurgijos gydytojas profesorius Audrius Šileikis.
Gydymo taktika parenkama individualiai – skirtingiems pacientams taikomi skirtingi chemoterapijos deriniai. Kadangi išskiriama keliolika biologinių kasos vėžio porūšių, jų reakcija į gydymą gali labai skirtis, taigi ir gydymo veiksmingumas kiekvienu atveju yra nevienodas.
„Nors imunoterapija sėkmingai taikoma kai kurioms kitoms vėžio formoms gydyti, kasos vėžio atveju jos veiksmingumas yra labai ribotas. Viena pagrindinių priežasčių – specifinė naviko mikroaplinka, kuri apsunkina vaistų patekimą į navikines ląsteles ir slopina imuninį atsaką“, – aiškina prof. A. Šileikis.
Todėl šiandien daug dėmesio skiriama kasos naviko mikroaplinkos tyrimams ir galimybėms ją paveikti.
Naujos kasos vėžio gydymo galimybės
Taikinių terapija yra vienas pažangiausių šiuolaikinės onkologijos metodų. Skirtingai nei chemoterapija, ji veikia konkrečius molekulinius procesus vėžinėse ląstelėse, todėl gali būti efektyvesnė ir mažiau žalinga sveikiems audiniams.
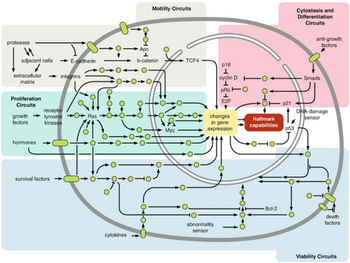
Vėžys išsivysto, kai dėl patologinių mutacijų organizmo ląstelės pradeda nekontroliuojamai dalintis ir plisti į kitus organus. Ląstelių dalijimąsi ir migraciją reguliuoja sudėtingas viduląstelinių signalų tinklas, o vėžys atsiranda sutrikus šiai reguliacijai.
Net to paties organo navikai gali susiformuoti dėl skirtingų molekulinių pokyčių. Didžiausias taikinių terapijos privalumas – galimybė gydymą parinkti pagal konkrečius sutrikimus, nustatomus paciento navike.
Taikinių terapija jau plačiai taikoma gydant kai kurias vėžio formas, pavyzdžiui, krūties vėžį. „Tačiau kasos vėžiui veiksmingų taikinių terapijos sprendimų vis dar beveik nėra – išimtis taikoma tik nedidelei daliai – maždaug 7 proc. – pacientų, turinčių BRCA1/2 genų mutacijų“, – teigia prof. A. Šileikis. BRCA1 ir BRCA2 genai yra vieni geriausiai ištirtų genų, kurių mutacijos didina krūties, kiaušidžių, prostatos ir kasos vėžio riziką.
VU GMC Proteomikos centro mokslininkai tiria, kokie molekuliniai pokyčiai lemia kasos vėžio vystymąsi ir kaip juos būtų galima paveikti vaistais, siekiant sustabdyti vėžinių ląstelių augimą ir kuo mažiau pakenkti sveikoms.
Tam pasitelkiama baltymų masių spektrometrija – pažangus metodas, leidžiantis „nuskaityti“ ląstelės baltymų profilį. Tiriamos tiek komercinės kasos vėžio ląstelių linijos, tiek iš pacientų navikų išvestos ląstelės. Vieno eksperimento metu galima identifikuoti iki 10 tūkst. baltymų ir nustatyti, kurie iš jų būdingi vėžiui ir kaip keičiasi jų aktyvumas.
Remiantis šiais duomenimis, ieškoma vaistų ar jų derinių, galinčių selektyviai veikti vėžines ląsteles. Jų veiksmingumas tikrinamas naudojant tas pačias ląstelių linijas.
Ypatingas dėmesys skiriamas vaistų perskirstymui (angl. drug repurposing) – strategijai, kai kitoms ligoms ar vėžio formoms gydyti jau naudojami vaistai pritaikomi kasos vėžiui. Toks požiūris leidžia sutrumpinti klinikinių tyrimų laiką ir sumažinti sąnaudas, todėl sėkmės atveju pacientus greičiau pasiektų jau ištirti ir saugūs vaistai.
Galiausiai, gydymą grindžiant molekulinių mechanizmų supratimu, atsiranda galimybė jį individualizuoti – parinkti kiekvienam pacientui tinkamiausią terapiją.
Kova su atsparumu chemoterapijai
Viena didžiausių problemų gydant vėžį, taip pat ir kasos, yra atsparumo chemoterapijai išsivystymas. Net ir iš pradžių veiksmingi vaistai ilgainiui gali prarasti efektyvumą, nes dalis vėžinių ląstelių išgyvena ir prisitaiko prie jų poveikio. Dėl to navikas gali atsinaujinti ar net tapti agresyvesnis.
VU GMC mokslininkai tiria, kokie molekuliniai mechanizmai lemia atsparumą plačiai taikomam chemoterapiniam vaistui oksaliplatinai ir kokie pokyčiai ar natūrali vėžinių ląstelių įvairovė nulemia šio atsparumo atsiradimą.
„Atsparumas vienam ar net keliems vaistams nėra absoliutus – jis susijęs su ląstelės reguliacijos ir medžiagų apykaitos pokyčiais, kurie gali būti išnaudoti kaip silpnoji vieta kuriant naujus terapinius sprendimus. Būtent tai ir yra šių tyrimų tikslas“, – pasakoja dr. M. Valius.
Kita naujoviška tyrimų kryptis – nustatant atsparumo susidarymo mechanizmus, parinkti vaistų derinius, galinčius užkirsti kelią atsparumo vystymuisi dar prieš jam atsirandant. Tokie sprendimai galėtų reikšmingai pagerinti gydymo efektyvumą, pacientų išgyvenamumą ir gyvenimo kokybę.
VU GMC ir Santaros klinikų įgyvendinamas projektas, finansuojamas Lietuvos mokslo tarybos (S-MIP-23-113), rodo, kad ateities vėžio gydymas bus vis labiau individualizuotas, tikslinis ir paremtas giliu ligos biologijos supratimu.